 Werbung
Werbung
| Strategie | Hebel | |||
| Steigender BioNTech SE ADR-Kurs | 5,13 | 6,72 | ||
| Fallender BioNTech SE ADR-Kurs | 4,38 | |||
|
hinterher.
AstraZeneca ist die jüngste der führenden Firmen im Rennen um einen Covid-19-Impfstoff, der seine Testverfahren, die so genannten Protokolle, veröffentlichen soll, hat aber die Endphase der Versuche außerhalb Großbritanniens noch nicht wieder aufgenommen und hinkt nun den Konkurrenten hinterher, sagen Analysten. Die AZN-Aktie fiel.
Das in Großbritannien ansässige Unternehmen AstraZeneca (AZN) veröffentlichte an diesem Wochenende die Protokolle, in denen die Phase-3-Studien für seinen Covid-19-Impfstoff beschrieben werden. Pfizer (PFE) und sein Partner BioNTech (BNTX) sowie Moderna (MRNA) haben ihre Phase-3-Protokolle letzte Woche veröffentlicht.
"Basierend auf den Protokollentwürfen gehen wir davon aus, dass PFE/BNT's BNT162b2 die Führung übernehmen wird, und je nachdem, wann die AZN-Studie wieder beginnt, könnte MRNA's mRNA-1273 folgen", sagte ein Analystenteam der Investmentbank SVB Leerink am Montag in einer Forschungsnotiz.
AstraZeneca war der erste Hersteller von Covid-19-Impfstoffen, der im Juli mit der Phase 3 oder Endphase der Versuche begann. Ende desselben Monats begannen auch Pfizer/BioNTech und Moderna mit Phase 3-Studien. Novavax (NVAX) und Johnson & Johnson (JNJ) kündigen an, dass sie noch in diesem Monat mit den Phase-3-Studien beginnen werden.
Ich denke, hier kommen mehrere Faktoren zusammen:
1. Kurskorrektur an den US-Börsen war imminent:
a.) September ist traditionell der schlechteste Börsenmonat.

https://www.aaii.com/journal/article/...patterns?printerfriendly=true
b.) Wahlen erhöhen Unsicherheit, damit Volatilität und von Anlegern geforderte implizite Risikoprämie. Im Ergebnis steigen die Cash-Bestände und sinken die Kurse. Eine OECD-weite Studie für die 1980er bis frühen 2000er hat statistisch eine Unterperformance der Börse für die Tage 25-3 vor einer Wahl, und Überperformance ab Tag 20 nach der Wahl nachgewiesen:
https://www.econstor.eu/bitstream/10419/22109/1/p22006.pdf
Ähnliche Analyse für die USA (1950-2016) hier
https://www.stocktradersalmanac.com/Alert/20161101.aspx
Im Schnitt S&P 500 -2% von Anfang Oktober bis 5 Tage vor der Wahl (-4%, falls amtierende Partei verliert, +-0, falls sie gewinnt - war übrigens 2016 der einzige Indikator, der Trumps Sieg korrekt vorhergesagt hat).
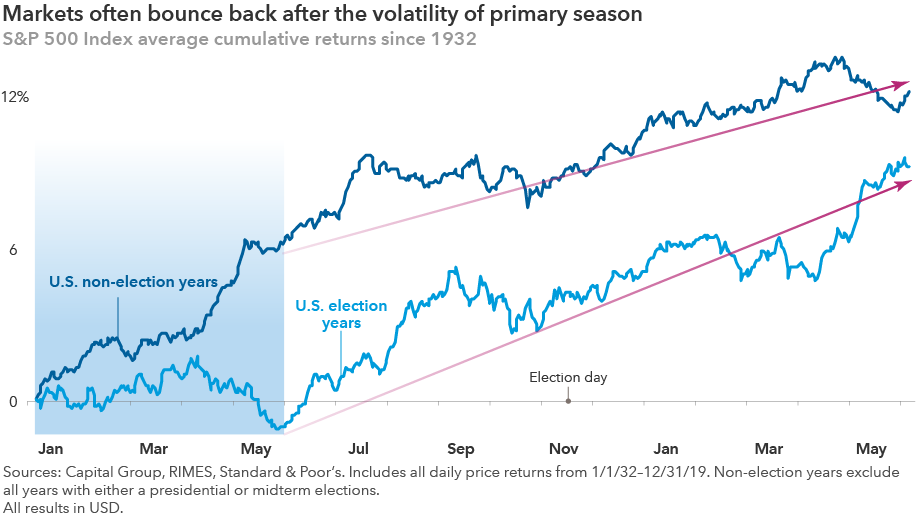
https://www.capitalgroup.com/advisor/ca/en/...akes-election-year.html
c.) Diese "Weisheiten" sind aktuell fast überall zu lesen (Beispiele verlinkt), und werden allein dadurch schon zur "self fulfilling prophecy".
https://edition.cnn.com/2020/08/17/investing/...ks-trading/index.html
https://am.jpmorgan.com/gb/en/asset-management/...ts/2020-us-election
https://www.bloombergquint.com/opinion/...sons-from-bush-vs-gore-2000
Man nehme dazu noch die offensichtliche Blasenbildung / Überbewertung infolge der Fed-Liquiditätsschwemme, et voila. Korrektur war also erwartbar. Einzig überraschend für mich ist der frühe Termin - ich hatte eher mit einem "Black Friday" gerechnet.
2. Die Impfstoff-Diskussion in den USA ist extrem politisiert. Insbesondere herrscht starkes Mißtrauen, das Trump die EUA eines nicht ausreichend getesteten Impfstoffs noch vor der Wahl durchdrücken könnte - und dies wäre dann BNT/Pfizers Impfstoff.
Physicians might refuse to administer a vaccine approved with inadequate data, said Dr. Preeti Malani, chief health officer and professor of medicine at the University of Michigan in Ann Arbor, in a recent webinar. You could have a safe, effective vaccine that no one wants to take. A recent KFF poll found that 54 percent of Americans would not submit to a Covid-19 vaccine authorized before Election Day."
https://www.nbcnews.com/health/health-news/...arm-scientists-n1240617
Wir haben es also aus US-Investorensicht mit zwei entgegengesetzten Zulassungsrisiken für BT/Pfizer zu tun:
a.) Die Zulassung könnte noch daran scheitern, dass unerwünschte Nebenwirkungen in Phase 3 auftauchen; oder
b.) Trump drückt "Notzulassung" gegen den Willen etwa der Hälfte der US-Bevölkerung durch, mit der Folge starker Impfverweigerung (54% lt. Umfragen) gegenüber diesem Impfstoff.
Gerade das zweite Risiko scheint mir z.Z. stark in den US-Kursen eingepreist zu werden. Da mag dann noch politisch motivierte Zurückhaltung hinzukommen: Genauso, wie ich aus politischen Gründen nie eine Rheinmetall-Aktie anfassen würde, mögen einige US-Investoren (z.B. in/um Hollywood) sich von Trumps "winner" fernhalten.
3. BioNTech als Corona-Titel ist noch nicht im Bewusstsein der US-Anleger verankert, sondern findet primär als "Anhängsel" von Pfizer Erwähnung - aktuellestes Beispiel, mal wieder mit dem klassischen Pfizer/Moderna/NovaVax Dreiklang, hier:
https://eu.usatoday.com/story/money/2020/09/21/...ne-leader/42634527/
Allerdings gibt es da Anzeichen eines Umdenkens. Besprechung von heute, mit Focus auf BNTX und Kursziel mindestens 105 USD:
https://moneymorning.com/2020/09/21/...e-doesnt-have-to-finish-first/
"That suggests the profit potential, if the mRNA vaccines succeed (and they don't have to be first, mind), for the stock to go at least as high as its old $105 high, and likely much further.
Mal schauen, was die anderen so in den nächsten Tagen schreiben..
https://seekingalpha.com/article/....stck.pro&utm_medium=referral
"Covid-19 Car Crash": Drei Themen (nicht in dieser Reihenfolge)
1. Rückschau auf AstraZeneca. U.a. weist der Artikel darauf hin, dass die letzten offiziellen AZ-Statements von "illnesses" und betroffenen "volunteers", jeweils im Plural, sprechen. Er schließt daraus auf mehr als nur einen Einzelfall. Darüber hinaus deuteten sonstige AZ-Veröffentlichungen darauf hin, dass zum Zeitpunkt des "Zwischenfalls" wohl erst 10 Probanden eine Zweitimpfung erhalten hatten. Das Auftreten einer ernsten, unerwarteten Komplikation bei einem vom 10 Zweitgeimpften wöge naturgemäß sehr viel schwerer, als Komplikationen unter gut 10.000 Erstgeimpften. Generell mahnt er noch ausstehende "details, details" von AZ an:
"Clearly, there is huge reluctance (in part because of massive political interference) to suggest that there might be a problem with the vaccine. (..) The confronting point is that the vaccine used in the Phase 3 trial has already been scaled up and is being manufactured. Of course, this never happens in normal vaccine development, because only after safety and effectiveness have been established does a finished version of the vaccine get scaled up. One can see why there is huge resistance to acknowledging that there might be a problem."
Bottom line: Bei AZ ist wohl mehr schiefgegangen, als AZ selbst, und die britischen Aufsichtsbehörden, eingestehen wollen. Diese Zurückhaltung mag mit den schon erheblichen Vorinvestitionen zusammenhängen. Das so entstandene Glaubwürdigkeitsproblem ist massiv.
2. "Political interference is a real problem": Muss ich vermutlich nicht übersetzen, Die im Artikel wiedergegebenen entsprechenden Statements der Trump-Administration wurden hier auch schon gepostet.
"The point is that the public understands what is going on. Vaccines need public acceptance and support or they cant be effective (even if they are proved to be safe and efficacious). A recent poll makes clear that public support for a COVID-19 vaccine is wavering. In April, 72% of US adults said they would get a COVID-19 vaccine when available. This has fallen 21 points to 51% today, with a significant part of this fall (8%) happening in the past month as the independence of the FDA from political interference has become a headline issue. This fall in intention is similar for both Republicans and Democrats. Another poll has just 39% of respondents saying that they would get a Government approved COVID-19 vaccine, with 23% saying no and 36% unsure.
The above numbers are not enough to achieve successful population-wide protection even based on a very effective vaccine."
Noch ein Glaubwürdigkeitsproblem, diesmal von Trump geschaffen. Die zitierten Umfrageergebnisse sind sogar noch schlechter als die aus meinem vorherigen Link.
3. Pfizer und Moderna arbeiten an ihrer Glaubwürdigkeit, aber traut die amerikanische Öffentlichkeit ihnen? Berichtet wird u.a. von der "Selbstverpflichtung" der "grossen Neun", und von den kürzlich veröffentlichten Studienprotokollen. Jedoch: "It is not yet clear how AstraZeneca, Pfizer or Moderna plan to be more transparent about adverse events."
Schlußfolgerung des Autors:
"My take at the moment remains that we dont have sufficient information to know if it will be possible to develop a safe and effective COVID-19 vaccine. If this proves possible, when such a vaccine might become generally available is also unclear, although it is almost certain that the second half of 2021 is the earliest it might become available, unless safety is disregarded and an unvalidated vaccine just gets pushed out. Even if this happens, I suspect the public will be cautious and not enough people will accept it to make it effective. I suspect that the vaccine developers know that they must re-establish public confidence in the vaccine development process, and Pfizer and Moderna have made a start. AstraZeneca says it will, but currently there are unanswered questions (..)"
Meine Kurzfassung/ Interpretation: Die hier vor ein paar Tagen von jemand anderem vorgebrachte These der "Sippenhaft" schlägt offensichtlich zu, und beschädigt nicht nur AZ, sondern auch andere Kandidaten einschließlich BT/Pfizer. Die Trump-Administration ist diesbezüglich alles andere als hilfreich. Das Resultat ist erhöhte Skepsis gegenüber allen Impfstoffkandidaten (und deren Zeitplänen). Eine Riesen-PR-Aufgabe, die Pfizer und Moderna (interessante Allianz hier, btw.) begonnen haben, anzugehen, mit bislang ungewissem Ausgang.
Dazu zwei Kommentare von https://stocktwits.com/symbol/BNTX:
$AZN$INO$NVAX$BNTX Look Trump crossed off AZN early this morning, he said get out now.
$BNTX Down this morning because Trump has been exposed by his Oracle/TikTok ultimatum and by his own words with Woodward and anything this man touches will turn to shit from here on out. God help us if he wins in November.
[Hoffe nicht, dass der Kommentator mit seiner Prognose, alles, was Trump anfasst, würde zu sh..t, bei BioNTech recht behält].
Ansonsten, optimistischer:
https://finance.yahoo.com/news/...tocks-poised-massive-122346468.html
Die drei genannten Kandidaten mit massivem Wachstumspotential sind Moderna, Novavax und BioNTech. Weder Kursprognosen noch klar geäusserte Präferenz. Jedoch, zu Biontech:
"Apart from research into coronavirus vaccine, BioNTech also owns several properties that provide in vitro diagnostic testing devices in the biopharma sector. The company has a compelling pipeline of immunotherapies for various cancers in the research and development stage. Many analysts are quick to tie the companys prospects to its deal with Pfizer. This can be quite misleading. One area which has been overlooked by analysts is the knowledge transfer implications that pandemic has for BioNTech. The deal with Pfizer would develop the company's ability and expertise to produce future inoculations for infectious disease without outside assistance.
This means that after the hype of the coronavirus vaccine has fizzled out; BioNTech can still be profitable with the array of products in the pipeline and develop its knowledge resource and expertise. This no doubt places the stock for an upward surge in the market."
könnte die Rivalen vorzeitig besiegen.
Die von Pfizer Inc. und seinem deutschen Partner BioNTech SE geplante Covid-19-Impfstoffstudie könnte es ihnen ermöglichen, vor ihren schnellsten Rivalen herauszufinden, ob ihre Impfung wirkt.
Die Unternehmen planen einen ersten Blick nach nur 32 Coronavirus-Infektionen, die sich in ihrer massiven, 44.000 Personen umfassenden Studie angesammelt haben. Diese Zahl könnte laut Airfinity Ltd., einer in London ansässigen Analytikfirma, die Impfstoffversuche verfolgt, bereits am 27. September erreicht werden.
Pfizer hat sich zudem vier Chancen auf ein vorläufiges Ergebnis eingeräumt, bevor das Endziel von 164 erreicht wird. Einige Studienexperten sagen, das Unternehmen scheine in einem Wettlauf mit Spitzenreitern wie Moderna Inc. und AstraZeneca Plc. um den ersten Platz bei einem Impfstoff zu suchen.
"Ich habe noch nie eine Studie gesehen, bei der es vier Zwischenanalysen gab; das könnte der olympische Rekord sein", sagte Eric Topol, Chefredakteur von Medscape, einer Website mit klinischen Informationen für Fachleute im Gesundheitswesen, und Direktor des Scripps Research Translational Institute in La Jolla, Kalifornien. "Es ist offensichtlich, warum das gemacht wird: damit man sich die Daten einfach weiter ansehen kann, um zu versuchen, ein Rennen zu gewinnen.
Ein breites Spektrum von Symptomen und Schweregraden macht die Bewertung von Covid-19-Impfstoffen schwierig. Die U.S. Food and Drug Administration hat erklärt, dass Impfstoffe, um zugelassen zu werden, die Zahl der symptomatischen Fälle um die Hälfte reduzieren müssten. Die von den Arzneimittelherstellern veröffentlichten Dokumente zeigen jedoch, dass jeder seinen eigenen Ansatz hat, um zu definieren, welche Symptome zählen und wann sie zu zählen sind.
Große Arzneimittelstudien ermöglichen es in der Regel einem Gremium von Monitoren, ein oder zwei Mal vor dem geplanten Ende einen frühen Blick auf die Daten zu werfen. Das Gremium kann die Studie vorzeitig abbrechen, wenn eine Behandlung als überwältigend wirksam beurteilt wird - oder alternativ, wenn sie als totaler Blindgänger gilt. Das Thema gewinnt zunehmend an Aufmerksamkeit, da Fragen über die Einstellung der Versuche von AstraZeneca am Menschen in den USA nach dem Auftreten von Nebenwirkungen, die laut Oxford wahrscheinlich nicht mit dem Impfstoff in Verbindung gebracht werden können, weiterhin bestehen.
Moderna, die mit dem National Institute of Allergy and Infectious Diseases der USA zusammenarbeitet, wird erst nach 53 Fällen einspringen; ihr Endziel ist es, bei 151 Diagnosen ein Urteil zu fällen. Das Krebs-Kraftpaket AstraZeneca, das mit der Universität Oxford zusammenarbeitet, wird erstmals 75 Fälle unter die Lupe nehmen und erst wieder, wenn die Studie mit 150 Fällen abgeschlossen ist.
"Alle Studien haben die Messlatte für das, woran sie getestet werden, ziemlich niedrig angesetzt", sagte Rasmus Bech Hansen, Chief Executive Officer von Airfinity.
Die Studie von Pfizer war so angelegt, dass ihr Impfstoffkandidat "so schnell wie möglich" evaluiert werden sollte, sagte Amy Rose, eine Sprecherin, in einer E-Mail. Das Unternehmen habe mit Wissenschaftlern der Regierung zusammengearbeitet, um bewährte Verfahren für Tests zu entwickeln, und seinen Zeitplan für Zwischenanalysen auf das "starke Profil" des Impfstoffs in frühen Human- und Tierversuchen gestützt, sagte sie.
Modernas Plan sei mit den US-Regulierungsbehörden vereinbart worden, und das Unternehmen habe die Zahlen schon vor Beginn der Studie Ende Juli bekannt gegeben, sagte Sprecher Ray Jordan in einer E-Mail. Die Gesamtzahlen der Fälle für die Zwischenanalyse basierten auf Erfolgswahrscheinlichkeiten und "wurden nicht aufgrund des Zeitrahmens ausgewählt", sagte er.
AstraZeneca sagte, dass ihre Studien unter behördlicher Aufsicht durchgeführt werden und ihre Pläne sich im Laufe der Zeit weiterentwickelt haben, um sicherzustellen, dass sie zeitnah robuste Informationen liefern. Alle Unternehmen sagten, dass ihre Studien über Punkte wie eine vorläufige Auslesung oder eine mögliche Zulassung hinaus fortgesetzt werden.
Pfizer sagt, dass ihre Studie wahrscheinlich im Oktober schlüssige Ergebnisse liefern wird. Keiner der Arzneimittelhersteller wird laut Airfinity wahrscheinlich wissen, ob ihre Impfstoffe die Krankenhauseinweisungen bis Februar verringern. Aber es sind die früheren Einschätzungen, die Beobachter am meisten beunruhigen.
Behandlungen wie das antivirale Remedesivir von Gilead Sciences Inc. und Rekonvaleszenzplasma - eine Suppe aus Immunfaktoren, die aus dem Blut von genesenen Covid-19-Patienten gewonnen wird - wurden bereits auf der Grundlage einiger begrenzter Daten zugelassen.
Diese werden jedoch hauptsächlich an extrem kranke Patienten verabreicht, deren Leben in Gefahr ist. Die Zulassung eines Impfstoffs hingegen könnte dazu führen, dass er bei Hunderten von Millionen nicht infizierten Menschen eingesetzt wird. Wenn das geschieht, dürften die Daten ziemlich überzeugend sein.
"Eine kleine Anzahl zusätzlicher Ereignisse, die eintreten oder nicht eintreten, kann die Bilanz einer Studie darüber kippen, ob die Ergebnisse gültig sind oder nicht", sagte Jonathan Kimmelman, Direktor der Abteilung für biomedizinische Ethik an der McGill-Universität in Montreal. "Wenn man robuste und verallgemeinerbare Ergebnisse haben will, sollte man eine angemessene Anzahl von Ereignissen akkumulieren".
Einige Impfstoffe werden zugelassen, nachdem nur wenige Fälle in Studien aufgetreten sind. Der Ebola-Impfstoff von Merck & Co. wurde im vergangenen Jahr auf der Grundlage einer Studie mit 3.500 Patienten zugelassen, bei der laut Etikett 10 Fälle festgestellt wurden. Aber diese Spritze hatte eine perfekte Wirksamkeit und sollte eine Krankheit mit einer himmelhohen Sterblichkeitsrate verhindern.
Milliarden von gesunden Menschen auf der ganzen Welt mit geringem Risiko für lebensbedrohliche Krankheiten könnten eine Coronavirus-Spritze erhalten, was die Messlatte für die Sicherheit höher legen würde. Eine Zulassung, die auf frühen Ergebnissen beruht, könnte bedeuten, dass Ärzte sehr wenig über einen Impfstoff wissen, abgesehen von den nackten Ergebnissen.
Würde der Impfstoff von Pfizer auf der Grundlage der Ergebnisse vom Oktober beispielsweise eine Notfallzulassung erhalten, hätten die meisten Patienten weniger als zwei Monate Nachbeobachtungszeit gehabt. Zu diesem Zeitpunkt wird nur wenig über die Dauer des Impfschutzes bekannt sein, und die Auswirkungen auf schwere Krankheiten sind möglicherweise nicht klar.
Neben einem positiven Test auf das Coronavirus erfordert Moderna, dass die meisten Patienten zwei oder mehr Symptome aufweisen, um die Wirksamkeit des Impfstoffs beurteilen zu können, es sei denn, sie haben einen verräterischen Marker wie Atemnot.
Die Studie von Pfizer geht jedoch tiefer in Patienten mit leicht symptomatischen Fällen. Sie zählt offiziell sogar einen Coronavirus-positiven Patienten mit Fieber allein, einer der häufigsten Manifestationen der Krankheit, zu den symptomatischen Fällen.
Dadurch kann Pfizer die Fälle möglicherweise schneller erfassen, aber es könnte auch ein frühes Ergebnis bedeuten, das hauptsächlich auf milden Fällen beruht, so Hansen von Airfinity.
"Wir sollten wirklich Krankenhausaufenthalte oder Todesfälle als Endpunkte haben, weil wir letztlich verhindern wollen, dass Menschen ernsthaft krank werden", sagte er.
Der Ansturm auf Ergebnisse könnte es schwieriger machen, klare Antworten darüber zu erhalten, wie gut die Impfstoffe wirken, sagte Topol, der Wissenschaftler von Scripps.
"Wir wollen wissen, ob dieser Impfstoff eine starke Wirksamkeit hat", sagte er. "Und das bedeutet zweierlei: dass er bei der Mehrheit der Menschen wirkt und dass er schwere Infektionen verhindert und nicht Hals- oder Muskelschmerzen.
Übersetzt mit www.DeepL.com/Translator (kostenlose Version)
|
 Werbung
Werbung
| Strategie | Hebel | |||
| Steigender BioNTech SE ADR-Kurs | 5,13 | 6,72 | ||
| Fallender BioNTech SE ADR-Kurs | 4,38 | |||
| Wertung | Antworten | Thema | Verfasser | letzter Verfasser | letzter Beitrag | |
| 79 | 32.125 | Biontech & MRNA: Revolution in der Pharmaindustrie | 51Mio | lordslowhand | 05.03.26 21:32 | |
| 71 | 57.806 | Biotech-Star BioNTech aus Mainz | moneywork4me | Balkonien | 05.03.26 20:04 | |
| 189 | BNTX | sellongoodnews | sellongoodnews | 03.09.25 09:51 | ||
| 5 | 791 | Translate Bio - mRNA der Zukunft? | Jack in the Box | Trader13 | 20.05.25 17:15 | |
| 23 | Einige User hier haben ein grundsätzliches Problem | Norbert Nebenwerth | Norbert Nebenwerth | 07.01.24 16:06 |