BioNTech forscht intensiv an mRNA-Krebsimpfstoffen.
Die EMA, hat den Produktkandidaten BNT211 für Patienten
mit stark vorbehandeltem Hodenkrebs für ein
beschleunigtes Zulassungsverfahren im Juli 2022 zugelassen
Die Europäische Arzneimittelagentur (EMA) hat BNT 211
den sogenannten PRIME-Status verliehen.
CAR-T-Zellen = Chimärer Antigen-Rezeptor
Der PRIME-Status der EMA unterstützt beschleunigte Zulassung
PRIME steht für PRIority MEdicines und hat zum Ziel
vielversprechende neue Medikamente für bisher
ungedeckten medizinischen Bedarf beschleunigt zuzulassen.
Im Rahmen des PRIME-Status kann BioNTech auf
wissenschaftliche Beratung und Unterstützung
der EMA zurückgreifen, um schnellstmöglich einen
Zulassungsantrag mit geeigneten Daten stellen zu können.
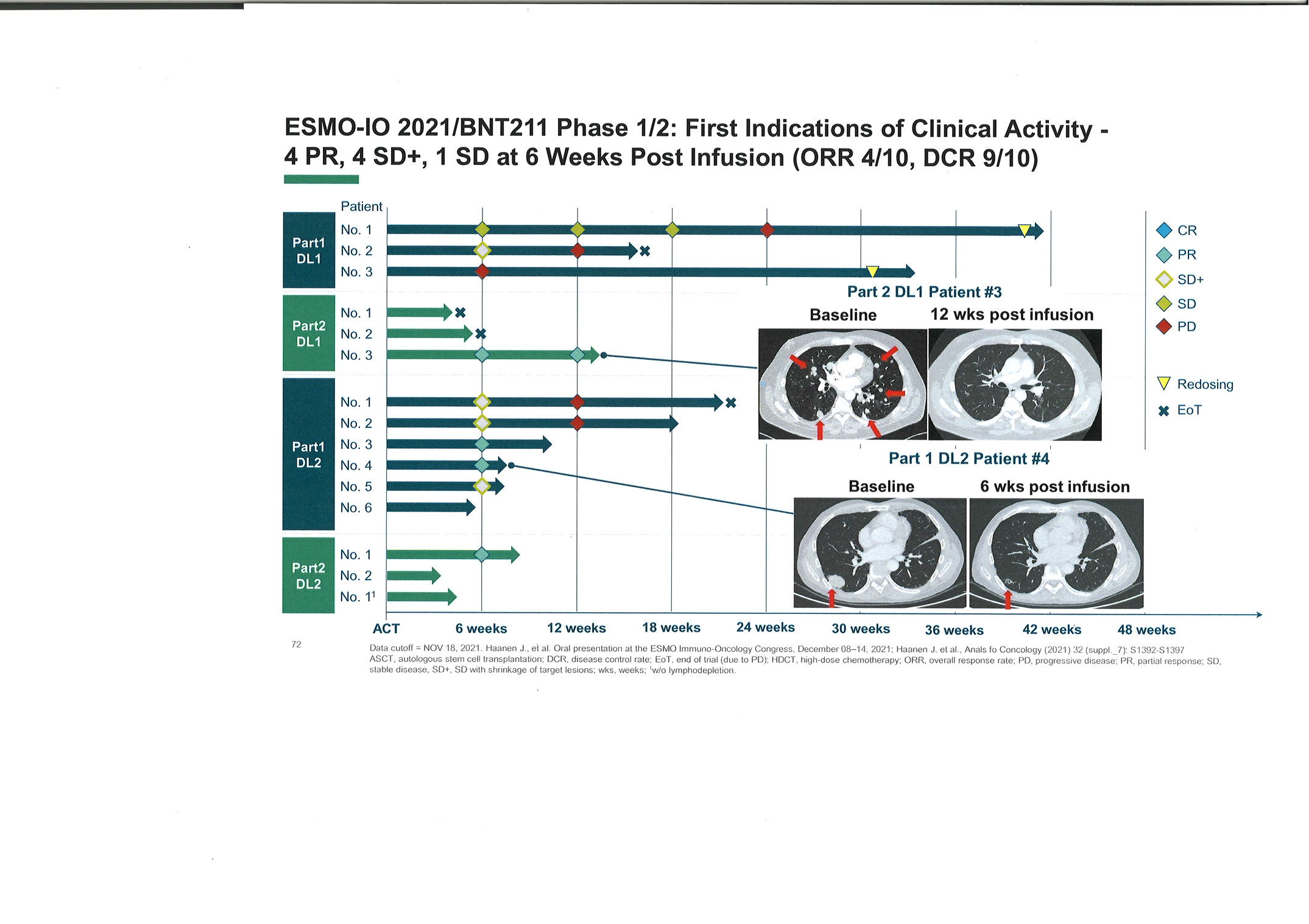
Auf der Jahrestagung der AACR 2021
präsentierte BioNTech Daten aus einer Phase-I/II-Studie
zu einer innovativen Therapie mit BNT211,
einer CAR-T-Zell-Therapie in Kombination mit einem
verstärkenden mRNA-Impfstoff (CARVac),
Die CAR-T-Therapie ist eine neuartige Form
der Tumortherapie, die Aspekte der Immun-,
Zell- und Gentherapie vereint.
CAR-T bedeutet Chimäre Antigenrezeptor-T-Zellen
und steht für gentechnisch veränderte T-Zell-Rezeptoren,
die auf Tumorzellen exprimierte Antigene erkennen und binden.
Die innovative Behandlung von BioNTech kombiniert
eine autologe CAR-T-Zell-Therapie, die sich gegen das
Membranprotein Claudin 6 (CLDN6) richtet,
mit der mRNA-Vakzine CARVac.
CARVac unterstützt dabei die CAR-T-Zell-Therapie,
indem es kontinuierlich aktivierend wirkt.
Bei CARVac handelt es sich um einen Nanopartikel-RNA-Impfstoff,
der für einen chimären CLDN6-Rezeptor kodiert.
Dadurch soll die CLDN6-Expession auf dendritischen Zellen
stimuliert und die Wirkung der CLDN6-spezifischen CAR-T-Zellen
verstärkt werden.
Es liegen Wirksamkeitsanzeichen bei Hodenkarzinom vor !
Die von BioNTech vorgestellten Ergebnisse beziehen
sich auf die Daten von 16 Patienten mit soliden Tumoren
wie Hodenkrebs, Eierstockkrebs und Gebärmutterkrebs,
die die CAR-T-Zell-Therapie als Monotherapie oder in
Kombination mit CARVac erhielten.
Sowohl die Mono- als auch die Kombinationstherapie
wiesen in beiden Dosisstufen ein gutes Verträglichkeitsprofil auf
und zeigten bei Patienten mit Hodenkrebs erste ermutigende
Hinweise auf eine klinische Wirksamkeit.
Alle sechs Patienten mit stark vorbehandeltem Hodenkrebs,
deren Daten ausgewertet wurden, zeigten Anzeichen einer
positiven klinischen Entwicklung. Einer der Patienten wies
18 Wochen nach der Infusion eine vollständige Remission (
complete response, „CR“) auf und drei Patienten zeigten ein
teilweises Ansprechen (partial response, „PR“).
BioNTech forscht nicht nur an BNT211,
sondern arbeitet an mehreren verschiedenen Immuntherapien
zur Tumorbekämpfung.
Einem weiteren Therapiekandidaten des Unternehmens BNT111
hat die amerikanische Zulassungsbehörde FDA (Food and Drug Administration)
im letzten Jahr ebenfalls einen bevorzugten Status, den Fast-Track-Status, verliehen.
Auch das Fast-Track-Programm soll dazu dienen,
Unternehmen bei einem beschleunigten Zulassungsverfahren
zu unterstützen.
Quelle Autor:
Franziska Zidek (Ärztin)
(Verkleinert auf 26%)